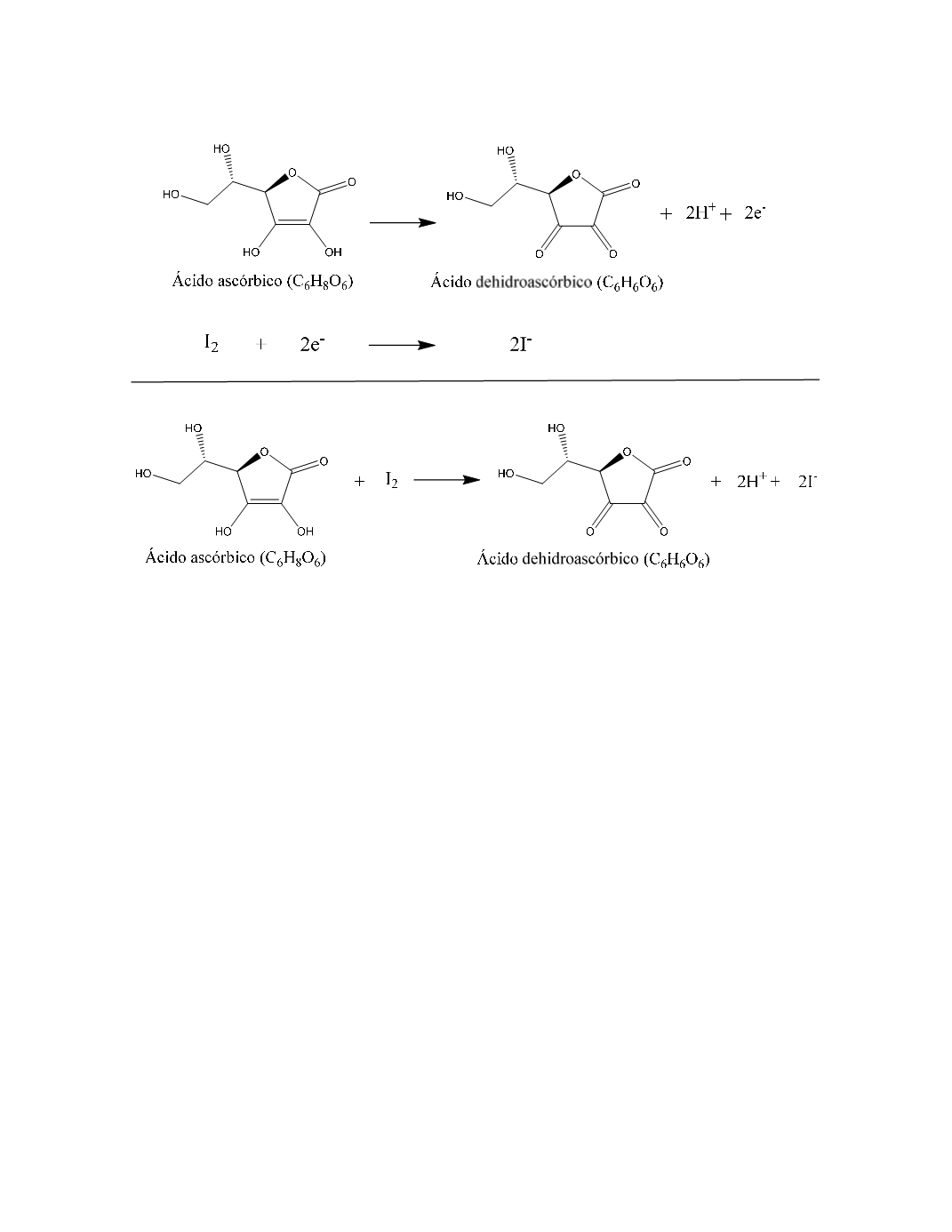
Figura 1. Reacción de oxidación del ácido ascórbico.
Las titulaciones en las que interviene el yodo como agente oxidante se denominan
yodimetrías. La reacción entre el yodo y el ácido ascórbico presenta una estequiometria
1:1. En el punto de equivalencia de la titulación, el número de moles de yodo reducidos es
igual a los moles de ácido ascórbico oxidados, es decir, el yodo es reducido a yoduro
mientras haya ácido ascórbico en la solución. Una vez que todo el ácido ascórbico se oxidó,
el yodo en exceso reacciona con un indicador de almidón, formando un complejo de color
azul oscuro en el punto de equivalencia.
El almidón se hidroliza con facilidad y uno de los productos obtenidos es la glucosa, la cual
tiene un carácter reductor, por lo que debe considerarse que una solución de almidón
parcialmente hidrolizada puede ser una fuente de error en una titulación redox.
En una titulación yodimétrica se determina la capacidad reductora total de la solución. Si
están presentes otras sustancias reductoras, además del ácido ascórbico, el volumen
consumido de la solución oxidante (yodo) será mayor y la concentración de ácido ascórbico
será sobrestimada. La vitamina C se oxida fácilmente en el aire, por lo que las disoluciones
de ácido ascórbico deben ser preparadas inmediatamente antes de ser tituladas.


